Investir dans l’Industrie des Dispositifs Médicaux en Chine
 Écrit par: Zhou Qian, Kyle Freeman et Matthew Zito
Écrit par: Zhou Qian, Kyle Freeman et Matthew Zito
Traduit par: Mathilde Veyrat
Investir dans l’industrie des équipements médicaux en Chine nécessite une bonne connaissance des règlements clés régissant le secteur, en particulier les procédures complexes et singulières pour obtenir un permis d’exploitation. Dans cet article, nous vous présentons quelques-unes de ces réglementations ainsi que les dernières informations concernant la place du secteur des équipements médicaux dans le Catalogue des industries pour guider l’investissement étranger.
Nouvelle réglementation relative aux dispositifs médicaux en Chine, effective depuis le 1er juin 2014 (Ordonnance 650).
C’est le dernier texte en vigueur présentant les modalités d’enregistrement des dispositifs médicaux, les exigences de fabrication et de distribution ainsi que la responsabilité en cas de comportement illégal. Par rapport au précédent texte de 2000, le nouveau règlement de 2014 propose les changements suivants:
- Amélioration du système de classification des risques
- Révocation des exigences relatives aux réenregistrements
- Facilitation du processus d’approbation pour encourager l’innovation
- Sanctions plus sévères en cas de violation
- Plus forte supervision après-vente
Réglementations de l’Administration de la Nourriture et des Médicaments
Pour soutenir la mise en place de l’ordonnance 650, l’Administration de la Nourriture et des Médicaments (China Food and Drugs Administration, CFDA en anglais) de Chine a adopté plusieurs textes de lois l’année dernière concernant l’enregistrement, la production et la distribution de matériel médical, parmi lesquels:
- Mesures administratives pour l’enregistrement des dispositifs médicaux (CFDA Ordonnance 4)
- Mesures administratives pour l’enregistrement des produits de diagnostic in-vitro (CFDA Ordonnance 5)
- Mesures administratives pour l’étiquetage des équipements médicaux (CFDA Ordonnance 6)
- Mesures administratives pour la supervision de la fabrication du matériel médical (CFDA Ordonnance 7)
- Mesures pour la supervision de la distribution du matériel médical (CFDA Ordonnance 8)
Le Catalogue des industries pour guider l’investissement étranger (Version de 2011)
Le Catalogue des industries pour guider l’investissement étranger est le document de référence publié par le Ministère du Commerce et la Commission Nationale pour le Développement et la Réforme. Il définit les restrictions/interdictions pour les investissements étrangers dans certains secteurs d’industrie en Chine. Concernant les dispositifs médicaux, l’édition de 2011 a levé les restrictions précédentes concernant la fabrication de seringues jetables, les sets de perfusion, les dispositifs de transfusion sanguine et les sacs de sang, ouvrant ainsi la voie pour toute sorte d’investissement étrangers dans le domaine médical.
![]() EN SAVOIR PLUS: Zoom sur le Marché des Dispositifs Médicaux en Chine
EN SAVOIR PLUS: Zoom sur le Marché des Dispositifs Médicaux en Chine
Le catalogue encourage aussi les investissements étrangers dans différents types de produits haut-de-gamme tels que les endoscopes éléctroniques, les rétinographes, les composants clés des équipements d’imagerie médicale, les transducteurs ultrasonores 3D, les équipements pour la thérapie par capture de neutrons par le bore (TCNB), les systèmes de radiothérapie avec modulation d’intensité guidée par l’image, les appareils pour dialyse et hémofiltration, ainsi que les dispositifs d’analyse d’immuno-essai automatisés.
De nouvelles révisions du catalogue ont été publiées sous la forme d’une ébauche soumise à l’opinion publique (date limite pour les commentaires fixée au 3 décembre 2014). Dans sa version actuelle, le catalogue inclut de nouveaux types d’équipements pour lesquels les investissements sont encouragés, notamment les analyseurs sanguins, les équipements d’immunoanalyse automatique par chimiluminescence et les systèmes de séquençage haut débit.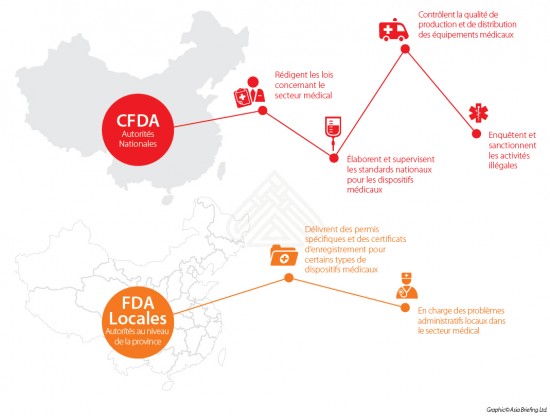
Autorités administratives et de supervision pour le secteur des équipements médicaux
En Chine, les autorités administratives et de supervision pour le secteur des dispositifs médicaux sont séparées selon deux niveaux. Au niveau national, l’Administration de la Nourriture et des Médicaments (CFDA en anglais) est en charge de la régulation et du contrôle du secteur des équipements médicaux pour l’ensemble du territoire.
En pratique, la CFDA délègue un grand nombre de tâches administratives à ses antennes locales, les FDA (Food and Drug Administration) présentes dans chaque province, région autonome et les municipalités.
Ces organismes sont autorisés à délivrer des permis spécifiques ainsi que des certificats d’enregistrement auprès des entreprises d’équipement médical à l’échelle de la province. Pour les investisseurs étrangers, il est important de noter que les critères d’exigence requis par les bureaux locaux seront probablement plus spécifiques et détaillés que ceux requis par l’administration au niveau national. Ainsi, tous les critères, qu’ils soient locaux ou nationaux, doivent être respectés.
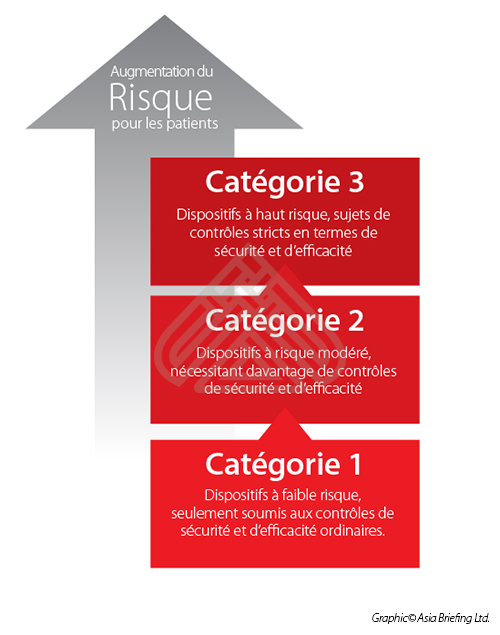 Classification des niveaux de risque
Classification des niveaux de risque
Le système de classification pour les dispositifs médicaux en Chine est considérablement différent de ceux de l’Union Européenne ou des Etats-Unis. Par exemple, un équipement considéré comme faisant partie de la catégorie 2 aux États-Unis ou de la catégorie 2-a/2-b dans l’UE pourra être considéré comme étant de la catégorie 3 en Chine, impliquant un processus d’enregistrement plus lourd et plus coûteux.
En Chine, la classification est définie selon l’ordonnance 15 de l’Administration de la Nourriture et des Médicaments ainsi que d’autres textes réglementaires. Bien que plusieurs facteurs complexes entrent en ligne de compte pour définir la classification d’un produit, on peut dire de façon générale que les équipements sont répartis en trois catégories en fonction du risque qu’ils présentent pour les patients ou les utilisateurs.
Résumé
Les investissements dans l’industrie des dispositifs médicaux en Chine promettent d’être très rentables dans les prochaines décennies à l’heure où on assiste à un vieillissement de la population. On recense aujourd’hui environ 194 millions de personnes âgées en Chine, chiffre qui devrait passer à 300 millions à l’horizon 2025. A cela s’ajoute le fait que les pensions de retraites chinoises sont très modestes, ce qui conduira la population active à montrer sa «piété filiale» et son respect des aînés en prenant soins des personnes âgées.
Alors que la classe moyenne chinoise devrait représenter près de 600 millions de personnes en 2025, le message est clair: les besoins en spécialistes de santé et d’équipements spécialisées pour les personnes du troisième âge vont exploser, tendance qui sera menée par les consommateurs de la classe moyenne. Investir dans le secteur n’est en revanche pas si simple qu’il n’y parait: divers permis spécifiques doivent être obtenus en fonction du secteur et du type de produit. Il est ainsi préférable pour les investisseurs intéressés par le potentiel de la Chine de se renseigner auprès de consultants spécialistes des questions règlementaires à l’entrée sur le marché.
|
Dezan Shira & Associates est un cabinet de conseils professionnels en matière d’investissement directs étrangers, gestion, fiscalité, comptabilité, paie et due diligence pour ses clients internationaux en Chine, à Hong Kong, au Vietnam et en Inde. Vous pouvez nous contacter à china@dezshira.com ou télécharger la brochure ici. Cet article est extrait de l’édition de Novembre 2014 du magazine China Briefing intitulé China Investment Roadmap: The Medical Device Industry, disponible en anglais dans notre bibliothèque. |
- Previous Article Zoom sur le Marché des Dispositifs Médicaux en Chine
- Next Article Cadre Juridique pour les Investissements dans L’Industrie des Dispositifs Médicaux en Chine